Kanser (malign neoplazi), çok hücreli canlıların büyük bir bölümünde karşılaşabileceğimiz belki de en gizemli hastalıklardan biri olarak karşımıza çıkmaktadır. Gün geçtikçe teknolojinin ilerlemesi ile birlikte artan
araştırmalar kanseri daha iyi bir şekilde anlamamıza ve çok çeşitli tedavi yöntemleri geliştirmemize olanak sağlamaktadır. Elbette herkesin kanser denilince az çok akıllarına bir şeyler gelmektedir fakat tam anlamı ile kanser nedir ?
Kanser “kusursuz” olarak atfedilen hücresel işleyişinin kendi doğası gereği sekteye uğramasından meydana gelen birtakım hatalar sonucunda hücrenin davranışlarının normalin dışına çıkmasına verilen isimdir. Yani daha kısa bir deyim ile “kontrolsüz hücre çoğalması”. Genellikle bu tür bir olayın yıkıcı etkilerini engellemek adına canlılar evrimsel süreç içerisinde bazı adaptasyonlar kazanmışlardır. Bu adaptasyonlardan en bilindiği hücre içerisinde çeşitli nedenler ile biriken bozulmanın hücre işleyişini bozabilecek seviyeye geldiğinde aktifleşen kendi kendini yok etme
mekanizması yani apoptoz tur. Fakat eğer ki bu intihar girişimi başarısız olursa hücre bütünlüğü bir anlamda bozulur ve kanserli hücre olarak adlandırdığımız mevcut hücre boyutlarını aşabilen ve normal bir hücreye göre çok daha fazla besin tüketme eğiliminde olan yepyeni hücreler meydana gelebilir.
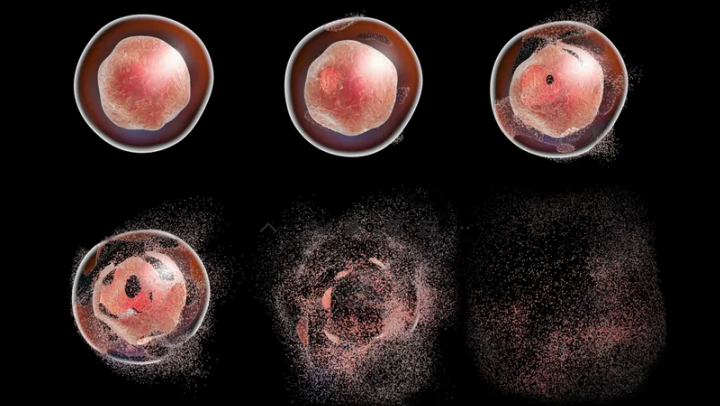
İşin güzel tarafı, vücudumuzda yer alan bağışıklık sistemi elemanları bu hücreleri önceden tanıyıp henüz çoğalmadan rahatlıkla yok edebilmeleridir. Ancak, hiçbir biyolojik süreç kusursuz değildir. Eğer kanserli hücre, bağışıklık sistemi elemanları tarafından yok edilmeden veya tespit edilmeden hızlıca çoğalmaya ve yayılmaya başlarsa, hatta aralarından birkaçı vücudun ücra köşelerine sığınıp bağışıklık sisteminden kaçabilirse, işte o zaman işler bizim için tehlikeli bir hâl almaya başlayabilir.
Tahmin edebileceğiniz üzere kanser, bizlerle aynı hücre tipine ve benzer organizasyona sahip tüm hayvanlarda ortaya çıkabilecek bir durumdur. Tüm hayvanların hücre boyutları aşağı yukarı bizimkine benzerdir; farklı olan, vücut büyüklüğüne bağlı olarak sahip olunan toplam hücre sayısıdır. Bu konuda verilebilecek en güzel örneklerden biri, fareler ve insanların karşılaştırılmasıdır. Bir insandaki toplam hücre sayısı, farelerdeki toplam hücre sayısının yaklaşık bin katıdır. Ancak ilginç olan, kansere yakalanma ihtimalinin insanlarda ve farelerde benzer oranlarda seyretmesidir.
Peki ya en büyük hayvan olarak bilinen mavi balinayı düşündüğümüzde? Bu canlı, bizimkinden yaklaşık 3.000 kat daha fazla hücreye sahiptir. Buna rağmen, mavi balinalarda kanserleşme oranı yok denecek kadar azdır. Yani, vücut büyüklüğü arttıkça kansere yakalanma riskinin de artması beklenirken, tam tersi bir durum gözlemlenmektedir. Bu mantığa aykırı görünen olguya biyolojide Peto paradoksu denir. Peto paradoksu, hücre sayısı arttıkça kanser görülme olasılığının artması beklenirken, vücut büyüklüğü ile kanser riski arasında belirgin bir ilişki olmaması durumudur.

Bilim insanları, bu paradoksu açıklamak için üç temel argüman öne sürmektedir. Bu argümanlardan ilki, evrimsel biyolojinin kapılarını aralamaktan; ikincisi, metabolizmayı anlamaktan; üçüncüsü ise “hipertümör” adı verilen yapıları incelemekten geçmektedir.
Onkogenler ve Tümör Baskılayıcı Genler
Evrimsel biyoloji, ilk bakışta mantıklı görünen bir şekilde, tek hücreden çok hücreliliğe geçişle birlikte artan hücre sayısına bağlı olarak hata yapma (ve dolayısıyla kansere yakalanma) riskimizin arttığını; buna karşılık, çok hücreli canlıların kanseri yenebilmek için daha fazla savunma mekanizması geliştirmesi gerektiğini öngörür. Bu adaptasyonları gerçekleştiremeyen bireyler, nesiller boyunca elenerek canlılık sahnesinden silinir. Böylece geride kalan bireyler, kansere dirençli gen bölgelerine sahip genomlarını nesiller boyunca aktarabilirler.
Tam da beklenildiği üzere, kansere dirençli gen bölgeleriyle ilgili olarak kromozomlarımızda “nokta atışı” yapabileceğimiz yerler vardır: proto-onkogen bölgeleri. Proto-onkogenler ve tümör baskılayıcı gen bölgeleri, kanserle doğrudan ilişkilidir. Eğer bu gen bölgelerinde bir mutasyon meydana gelirse, hücrede bazı mekanizmalar ters çalışmaya başlar. Bu durum hücreyi kanserleşmeye itebilir.
Kanserleşen hücre, bağışıklık sistemi elemanlarından korunabilir veya onlardan saklanabilir, vücudun farklı bölgelerine yayılabilir (metastaz) ve anjiyogenez adı verilen süreçle kendine besin sağlamak amacıyla yeni damar oluşumunu tetikleyebilir. Ayrıca, ilgili bölgedeki mutasyona bağlı olarak kanserli hücre, kendini adeta “ölümsüz” bir hâle getirebilir.
Fakat bahsettiğimiz üzere, evrimsel süreçte kanseri yenebilmek adına bazı adaptasyonlar geliştiren canlılar, bu tür bir durumun üstesinden gelebilmek için nesiller boyunca tümör baskılayıcı gen ailesi olarak adlandırılan kanser karşıtı genetik özelliklere sahip olmuştur. Bu elbette bir anda gerçekleşen bir durum değildi; “Hücrelerimiz kontrolden çıkıyor, hemen bir çözüm yolu üretelim ve DNA’nın mutasyona uğramış ya da hasar görmüş bölgelerini onaralım” demek mümkün değildi. Burada etkili olan en önemli mekanizma, daha önce bahsettiğimiz gibi doğal seçilimdi.
Kanserin yıkıcı etkisine hücresel yanıt veremeyen canlıların nesilleri tükenerek, kansere karşı dayanıksız gen bölgeleri zamanla ortadan kalktı. Buna karşılık, genetik yapıları sayesinde bağışıklık sistemi elemanları daha fazla ya da daha hassas olan bireyler, kanserli hücreleri daha iyi tespit edebildiler. Yine bazı bireyler, DNA hasarını çok daha etkili şekilde onarabilen proteinlere sahip olduklarından, kanserli hücrelerin temelinde yatan mutasyon gibi etkenlerin üstesinden çok daha hızlı gelebildiler. Tümör baskılayıcı genleri, işte bu tür işlevleri gerçekleştiren proteinleri kodlayan genler olarak düşünebilirsiniz.
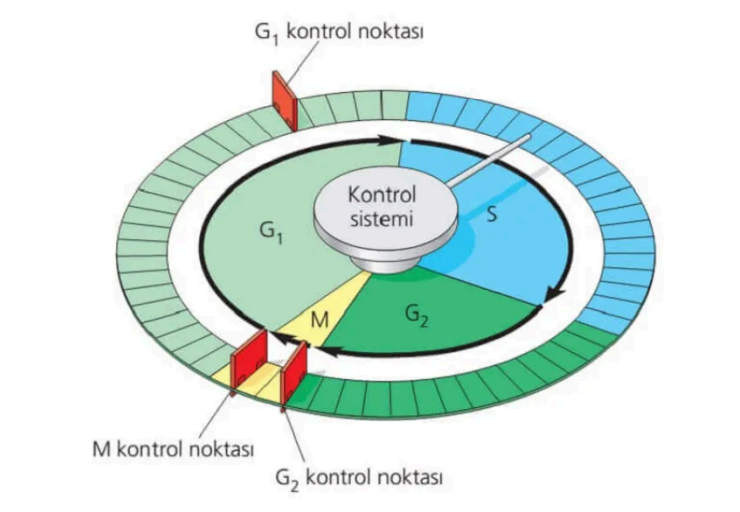
Bunlara ek olarak, hücrelerin “kontrol noktası” adı verilen bazı yapıları da vardır. Bunun en iyi örneklerinden biri tp53 gen bölgesidir. Bu genin ürettiği p53 proteini, hasarlı bir DNA bölgesi tespit edildiğinde hücrenin intihar mekanizmasını tetikler ve böylece hücrenin çoğalarak hasarlı DNA’sını aktarmasının önüne geçer. Devasa cüsseleriyle bilinen fillerde, p53 proteinini kodlayan tp53 gen bölgesinden 20 kopya bulunur. Bu tekrar sayısının fazla olması, hasarlı DNA’ya sahip hücreleri çok daha hızlı tanıyabilmelerini sağlayabilir; çünkü insanlarda yalnızca tek bir tp53 gen bölgesi vardır.
Fillerin bir diğer savunma mekanizması araştırıldığında ise, tp53 geni ile birlikte çalışan ve hasarlı hücreyi henüz kanserleşmeden ortadan kaldıran LIF6 geni keşfedilmiştir. Bu genin etkinliğini anlamak için, araştırmacılar fillerin bağ dokusu hücrelerini kimyasal bir yöntemle DNA hasarına maruz bırakmıştır. Bunun sonucunda LIF6 geninin normalden sekiz kat daha aktif rol aldığı gözlemlenmiştir. Ancak aynı deney tp53 geni inhibe edildiğinde, LIF6 geninin çalışmadığı belirlenmiştir.

Peki, Daha Büyük Hayvanlar Neden Bu Kadar Kanserleşmeye Dirençlidir?
Yapılan araştırmalar, yüksek kütleli hayvanların tümör baskılayıcı gen bölgelerine daha fazla sahip olduğunu ortaya koymuştur. Yani, bir mavi balinada bir hücrenin kanserleşebilmesi için DNA hasarının çok yüksek boyutlarda olması gerekir. Ancak, tümör baskılayıcı gen sayısının bizler gibi kendisinden çok daha küçük canlılara kıyasla çok daha fazla olması, kanserin işini oldukça zorlaştırır. Buradan çıkarılacak sonuç şudur: Bu canlıların genleri, diğer tüm canlılar gibi mutasyona uğrar; fakat bu mutasyonlar çok hızlı ve etkili biçimde tespit edilip onarılır. Nitekim, vücudumuzda her saniye hücre bölünmesi sırasında hatalar oluşur. Ancak bu hatalı hücreler, kontrol mekanizmalarından ve bağışıklık sisteminden geçemediği için biz fark etmeden yok edilir.
İkinci Argüman: Metabolizma
Bir diğer temel argüman ise metabolizma ile ilgilidir. Vücut büyüklüğü ile metabolizma arasında ters bir ilişki vardır. Canlının vücut büyüklüğü ve ağırlığı ne kadar düşükse, metabolizması (hücrelerdeki tüm kimyasal reaksiyonların hızı) o kadar yüksektir. Bu da daha fazla hücre bölünmesine ve dolayısıyla daha fazla hataya neden olabileceği düşüncesini beraberinde getirir. Oysa mavi balina gibi devasa hayvanların metabolizması son derece yavaştır; bu nedenle hata oranı da düşük olur. Bu durum, ömürleri boyunca kanserleşmeye yol açabilecek hücre sayısının azalmasına katkı sağlar.
Üçüncü Argüman: Hipertümörler
Gelelim üçüncü argümana: hipertümörler. Terim, köken olarak “hiperparazit” kavramından gelir; yani parazitlerin paraziti. Hipertümörde de durum benzerdir: Kanserli hücrelerin kanserleşmesi. Kanserli hücreler vücutta büyüyüp gelişirken kendi kopyalarını üretir; ancak bu kopyalar, ilk kanserli hücre gibi kusurludur ve birbirlerinden farklı özellikler taşır. Ortaya çıkan bazı yeni kanserli hücreler, diğerleriyle bir arada kalmak yerine ayrılıp daha fazla besin arayışına çıkar. Bu arayış genellikle, içinde bulundukları tümörün beslenmesini sağlayan kan damarlarına ulaşmalarıyla son bulur. Yeni hücreler kan damarlarına ulaştığında ise, eski kanser hücreleri beslenemez hâle gelir ve zamanla ölür. Bu döngü, yeni hücrelerin de aynı tehditle karşı karşıya kalmasına neden olur. Eğer bu durum sürekli tekrar ederse, tümörlerin kendi içlerindeki rekabet ve yok edici etkileri, vücudun korunmasında önemli bir unsur hâline gelir.
Dolayısıyla, devasa bir mavi balinada yüzlerce, binlerce, hatta milyonlarca kanserli hücre bulunabilir; ancak bu sayı, toplam hücre sayısına oranla çok küçük kalır. Bunu zihinde canlandırmak için şu örnek verilebilir: 4 gramlık kanser hücresi kitlesi, bir farenin toplam kütlesinin %20’sini oluştururken, bir insanın yalnızca %0,004’ünü oluşturur. Mavi balina söz konusu olduğunda ise bu oran çok daha küçüktür. Bu nedenle, devasa canlılar vücutlarında kanserli hücreler barındırsa bile, bu hücreler genellikle ciddi bir tehdit oluşturacak boyutlara ulaşamaz.
Tüm bunlara ek olarak, farklı canlı türlerinde hücre içi organizasyon ve içerik, farklı metabolik hızlarda işleyebilir. Eğer bu farklılıkların neye bağlı olduğu net olarak ortaya konulabilirse, belki de en zorlu düşmanımız olan kansere karşı çok daha etkili çözümler geliştirebiliriz.
Kaynaklar
- R. Peto. (2016). Epidemiology, Multistage Models, And Short-Term Mutagenicity Tests.
- M. Tollis, et al. (2019). Return To The Sea, Get Huge, Beat Cancer: An Analysis Of Cetacean Genomes Including An Assembly For The Humpback Whale (Megaptera Novaeangliae)
- M. Sulak, et al. (2016). Tp53 Copy Number Expansion Is Associated With The Evolution Of Increased Body Size And An Enhanced Dna Damage Response In Elephants
- S. Maciak, et al. (2015). Cell Size And Cancer: A New Solution To Peto’s Paradox?
Evrim Ağacı // 9 Şubat 2021




